
Хронічне запалення вирує в організмі, як пожежа. На щастя, вчені розробляють нові методи лікування. (Автор зображення: Ніколас Фордер)
Запалення є однією з надздібностей організму. Це допомагає нам боротися з інфекціями та загоювати рани.
«Якщо у вас немає запалення, ви помрете», — сказав Live Science Ед Райнгер, професор, який вивчає хронічне запалення в Бірмінгемському університеті у Великобританії. «Це так просто».
Але якщо воно переходить з короткочасної реакції на таку, що триває місяцями або роками, хронічне запалення може підживлювати такі захворювання, як цироз печінки, ревматоїдний артрит (РА) і хвороби серця.
У минулому лікарі намагалися лікувати ці захворювання, припиняючи всі запалення, що мало неприємні побічні ефекти та не завжди спрацьовувало. Але тепер вчені розробляють методи лікування, які не повністю усувають запалення, а перепрограмують клітини, які його живлять.
А при таких захворюваннях, як рак, коли пухлини захоплюють загоєння запалення, щоб підштовхнути свій ріст, нові методи лікування натомість застосовують протилежний підхід — повертають запалення до стану боротьби, щоб воно могло краще атакувати ці мутовані клітини.
Залежно від контексту запалення можна розглядати як корисне чи шкідливе, але завдяки новим дослідженням у будь-якому випадку його можна повернути під контроль.
«Якщо ви можете це зробити, ви можете дозволити імунній системі та запальній реакції продовжувати це робити, просто звичайним способом», — сказав Райнгер.
Гостре і хронічне запалення
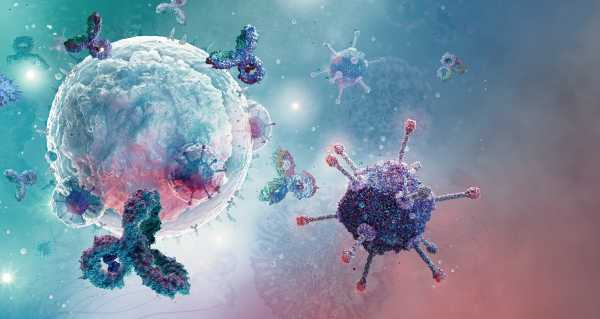
Лейкоцити, зображені вище, є ключовими учасниками запальної реакції організму на патогени.
Запалення є природною реакцією організму на фізичну травму, інфекцію або токсини, і лікарі описували його з давніх часів. «Inflammare» на латині означає «підпалити», і в другому столітті Гален, лікар римського імператора Марка Аврелія, описав його п'ять «кардинальних ознак» як жар, почервоніння, набряк, біль і втрата функції.
Те, що описували ці перші лікарі, було ознаками гострого запалення. Почервоніння та жар спричинені локальним розширенням кровоносних судин для передачі більшої кількості клітин до пошкодженої тканини, тоді як вивільнення таких сполук, як простагландини, викликає біль і набряк. Щоб перешкодити інфекціям, імунна система також виробляє хімічні речовини, які називаються пірогенами, які ще більше прискорюють вироблення простагландинів, викликаючи лихоманку.
«Вся суть запалення полягає в тому, щоб контролювати інфекцію, зупинити її поширення, а потім дозволити процесу загоєння початися», — сказав Live Science Роберт Ентоні, доцент медицини Гарвардського університету.
Під час гострого запалення пошкоджені клітини посилають сигнали «небезпеки», які заманюють імунні клітини до місця атаки. Ці перші реагують включають амебоподібні макрофаги, які поглинають шкідливих загарбників, і нейтрофіли, які вловлюють і вбивають цих ворогів. Після активації ці клітини виробляють хімічні речовини, які називаються цитокінами, які підсилюють запалення в циклі позитивного зворотного зв’язку.
У міру того, як це гостре запалення лютує, імунна система вчиться вибирати ворога більш вибірково.
Зазвичай гостре запалення досягає піку приблизно через сім днів після початкового нападу та починає зникати приблизно через три дні, сказав Ентоні. У той же час певні клітини працюють над загоєнням ран, виділяючи протизапальні сигнали та сприяючи утворенню нових кровоносних судин і сполучної тканини.
Суть запалення полягає в тому, щоб контролювати інфекцію, зупинити її поширення, а потім дозволити процесу загоєння початися
Роберт Ентоні, Гарвардський університет
Вчені до кінця не розуміють, як організм вимикає гостре запалення. Але іноді — наприклад, якщо імунна система не може повністю контролювати інфекцію — це не робить. Потім запалення може перетворитися з необхідного на шкідливе.
Якщо «ви зупините цей перехід приблизно на 10-й день, тоді все перейде в хронічну фазу», — сказав Ентоні.
При хронічному запаленні нейтрофіли, макрофаги та інші лейкоцити затримуються в місці запалення. Вони виробляють цитокіни, які пригнічують запалення. Запальні клітини також виробляють фактори росту, які підживлюють поділ клітин, і ферменти, які спричиняють пошкодження тканин, які потім надсилають більше сигналів «небезпеки», щоб зберегти цикл.
Хронічне запалення пов’язане з рядом захворювань, включаючи РА, який вражає суглоби; цироз печінки або серйозне рубцювання печінки; атеросклероз або бляшки в кровоносних судинах, які можуть призвести до інфаркту та інсульту. А клітинна проліферація та мутація, спричинені хронічним запаленням, можуть створити ідеальне середовище для розвитку раку.
Історична обробка

Преднізолон є поширеним кортикостероїдом. Як і інші в своєму класі, він може зменшити запалення, але має деякі небажані побічні ефекти.
У минулому лікування було спрямоване на те, щоб повністю заглушити запалення. Наприклад, у 1950-х роках вчені виявили протизапальну дію групи природних сполук, які називаються стероїдами, які зменшують гучність ширшої імунної відповіді. Відтоді стероїди стали основним засобом лікування хронічних запальних захворювань, таких як РА. Але на додаток до загального пригнічення імунної системи, стероїди можуть викликати такі побічні ефекти, як високий кров'яний тиск, виразка шлунка та перепади настрою.
Потім, у 1990-х роках, фармацевтичні компанії почали випуск ліків під назвою біопрепарати. Багато з них діють шляхом придушення різних цитокінів, хімічних сигналів, які підсилюють запалення.
Однак, як і стероїди, біологічні препарати часто пригнічують велику кількість імунної системи, що може збільшити ризик інфікування. Наприклад, препарат тофацитиніб для лікування ревматоїдного артриту націлений на сигнальний шлях, спільний для багатьох цитокінів, і, як наслідок, може зробити людей більш вразливими до вірусу оперізувального герпесу, пневмонії та інфекцій сечовивідних шляхів. І з причин, які ми не зовсім розуміємо, біопрепарати не працюють для кожного пацієнта.
Тому вчені шукають більш цілеспрямовані способи перенаправлення шкідливого запалення, часто шляхом перепрограмування імунних клітин, які беруть участь у цьому процесі.
Клітинне перепрограмування
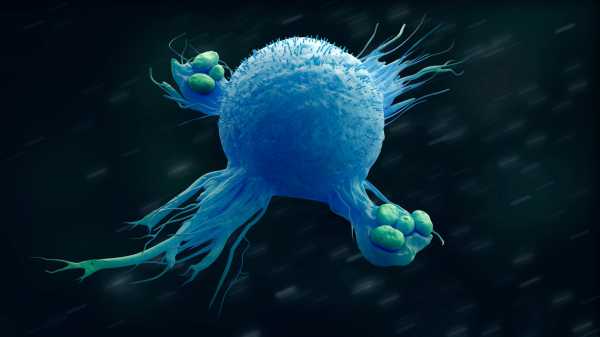
Ілюстрація макрофага, запальної клітини, схожої на Pac-Man, яка поглинає загарбників. Вчені виявили, що макрофаги існують у двох формах: ушкоджувальний запальний тип, який отримав назву М1, і другий тип, який називається М2, який сприяє регенерації тканин.
Стюарт Форбс, директор Центру регенеративної медицини та Інституту регенерації та відновлення Единбурзького університету у Великобританії, вивчав роль макрофагів у формуванні рубцевої тканини при фіброзі печінки. Він та інші виявили, що насправді існує два типи макрофагів: пошкоджуючий запальний тип, який отримав назву М1, і другий тип, який називається М2. Його дослідження на мишах виявили, що цей другий тип вимикав запалення та стимулював регенерацію тканин.
Тому команда Forbes відфільтровує клітини-попередники макрофагів, звані моноцитами, з крові пацієнтів із серйозними рубцями на печінці. У лабораторному посуді команда використовує хімічні сигнали, щоб підштовхнути ці моноцити до регенеративної версії M2. Потім дослідники вливають ці перепрограмовані макрофаги назад пацієнтам.
«Використовуючи наш підхід, ми намагаємося стимулювати регенерацію цих печінк, що означає руйнування рубцевої тканини, а це означає зміну запалення з запалення, яке викликає пошкодження, на запалення, яке формує відновлення», — сказав Forbes Live Science.
Цей підхід було визнано безпечним у фазі I клінічного випробування дев’яти пацієнтів у 2019 році, з «обнадійливими» результатами випробування ефективності фази II у 50 пацієнтів, представлених Forbes у листопаді на засіданні Американської асоціації з вивчення захворювань печінки, сказав він. Команда виявила, що протягом річного випробування лікування макрофагами зменшило кількість потенційно смертельних ускладнень, пов’язаних з печінкою, порівняно з контрольною групою, яка не отримувала лікування.
Тканиноспецифічні клітини
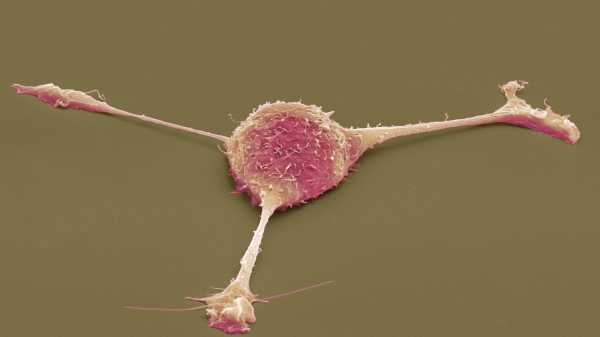
Зображення фібробласта скануючим електронним мікроскопом. Вчені дізналися, що різні типи фібробластів відіграють певну роль у розвитку ревматоїдного артриту та остеоартриту.
Однак, щоб лікувати кореневу проблему запальних захворювань, вам потрібно знати критичні клітини в певній тканині, сказав доктор Кріс Баклі, професор трансляційної ревматології в Оксфордському університеті, Live Science.
Наприклад, при РА лейкоцити, які є частиною адаптивної імунної системи, помилково націлюються на тканини суглобів. Ці лейкоцити активують макрофаги та клітини, що утворюють сполучну тканину, які називаються фібробластами, які викликають запалення суглобів. Типове лікування ревматоїдного артриту спрямоване на лейкоцити-ізгої. Проте лише 50% пацієнтів з РА досягають ремісії.
Але в статті 2019 року в журналі Nature Баклі та його колеги виявили, що один тип фібробластів у суглобі викликає запалення при ревматоїдному артриті, а інший — пошкодження кісток і хрящів при остеоартриті. Це підвищує перспективу лікування цих захворювань шляхом націлювання на фібробласти, унікальні для кожного захворювання: запальні фібробласти при ревматоїдному артриті та ті, що пошкоджують кістки та хрящі, при остеоартриті.
Для ревматоїдного артриту, наприклад, якби вони могли націлюватися як на лейкоцити, так і на фібробласти, вони могли б отримати 100% ремісію, сказав Баклі.
Лікування знаходиться на початковій стадії. Однак у 2021 році препарат під назвою селіцикліб, який пригнічує проліферацію фібробластів у суглобах, був визнаний безпечним під час клінічних випробувань фази I за участю 15 пацієнтів з ревматоїдним артритом, що відкриває шлях для майбутніх випробувань для оцінки ефективності препарату.
Роздмухування вогню назавжди
При деяких хронічних захворюваннях вчені розробляють методи лікування, які стимулюють запалення.
При раку, наприклад, макрофаги мігрують до пухлин і атакують їх, але ракові клітини захоплюють цей процес, вивільняючи хімічні речовини, які змушують макрофаги переходити з прозапального типу М1 на регенеративний тип М2, який пригнічує запалення та сприяє росту пухлини.
Озброївшись цими знаннями, доктор Яра Абду, доцент кафедри онкології в Університеті Північної Кароліни, та її колеги задалися питанням, чи можна використовувати вірус, щоб змусити макрофаги у хворих на рак більш схильні розпізнавати та атакувати пухлинні клітини, по суті діючи як макрофаги M1.
У 2022 році ранні результати триваючого клінічного випробування фази I за участю 18 пацієнтів із різними типами солідного раку — включно з раком молочної залози, яєчників і стравоходу — показали, що лікування цими перепрограмованими макрофагами під назвою CT-0508 було безпечним і мало багатообіцяючі результати.
«Ми також змогли побачити, що CT-0508 здатний викликати запалення мікрооточення пухлини», — сказав Абду в електронному листі Live Science. За її словами, ці макрофаги також рекрутували та активували інші імунні клітини, які мали завдання знищити рак.
Абду сказав, що більше даних із випробувань буде надано у 2024 році. Ґрунтуючись на цих «обнадійливих» результатах, команда також планує випробувати альтернативну версію цієї терапії під назвою CT-0525, яка використовує перепрограмовані моноцити замість макрофагів, у Фазі I клінічних випробувань у 2024 році.
Наступні кроки
Форбс і його колеги, маючи за плечима клінічні випробування II фази, хочуть випробувати вдосконалену версію своєї макрофагальної терапії на пацієнтів, які були госпіталізовані з цирозом печінки.
«На даний момент трансплантація печінки з довічним лікуванням є єдиним варіантом для пацієнтів із прогресуючим цирозом печінки», — сказав Forbes. Тому терапія макрофагами може забезпечити «новий терапевтичний варіант для цієї великої та зростаючої популяції пацієнтів».
Наразі трансплантація печінки з довічним доглядом є єдиним варіантом для пацієнтів із прогресуючим цирозом печінки
Стюарт Форбс, Единбурзький університет
На клітинному рівні Баклі хотів би дізнатися більше про те, що спонукає фібробласти як до запального стану, так і до стану пошкодження хряща, з’ясовуючи, чи ці дві форми розвиваються із загальної клітини-попередниці, і визначаючи, які фактори можуть регулювати цей процес.
Баклі та його колеги написали в оглядовій статті за 2021 рік, якщо знати більше про ці фібробласти, як у здоров’ї, так і при хворобі, можна «розкрити їхній терапевтичний потенціал у відновленні тканин».
За її словами, щодо терапії раку, яку розробляють Абду та її команда, залишається багато питань. Наприклад, команді необхідно точно налаштувати точну дозу, яку призначатимуть пацієнтам, і оцінити, проти якого типу раку вона може бути більш ефективною.
Проте вони сподіваються, що зможуть перейти до наступного етапу тестування, фази II клінічного випробування, і в разі успіху одного дня запровадити його на пацієнтів.
Зрештою, те, що Абду та інші роблять, це зміна способу, яким ми бачимо запалення; не лише як недолік, який потрібно виправити, а скоріше як неймовірна сила, якою можна керувати та використовувати назавжди.
ТЕМИ в центрі уваги науки

Emily CookeСоціальні посилання NavigationStaff Writer
Емілі – автор новин про здоров’я, живе в Лондоні, Велика Британія. Вона має ступінь бакалавра з біології в Даремському університеті та ступінь магістра з клінічної та терапевтичної неврології в Оксфордському університеті. Вона працювала в сфері наукових комунікацій, писала медичні статті та була репортером місцевих новин, одночасно проходячи навчання з журналістики NCTJ у News Associates. У 2018 році її назвали одним із 30 журналістів MHP Communications, за якими варто стежити молодше 30 років. (emily.cooke@futurenet.com)
Sourse: www.livescience.com


